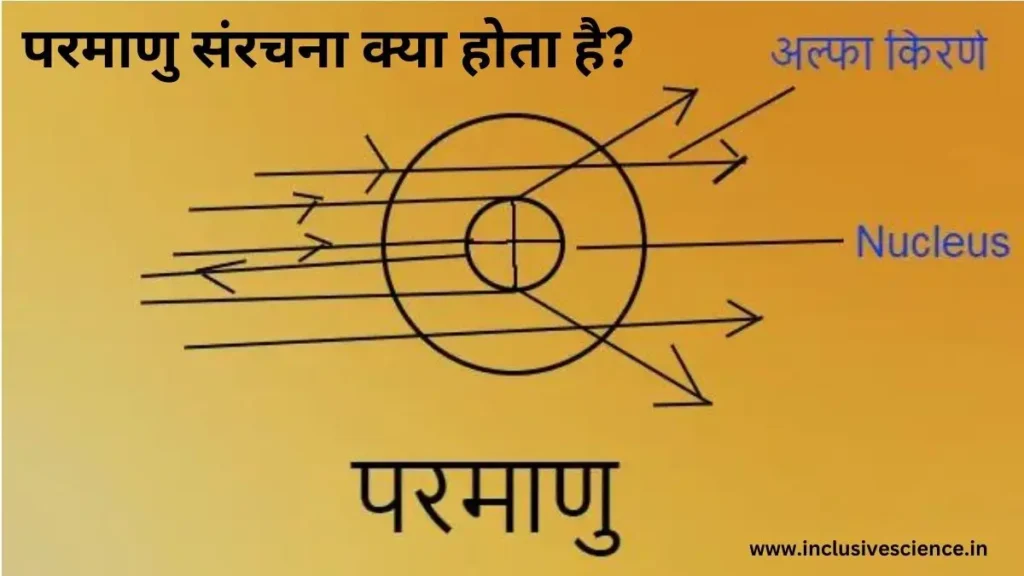
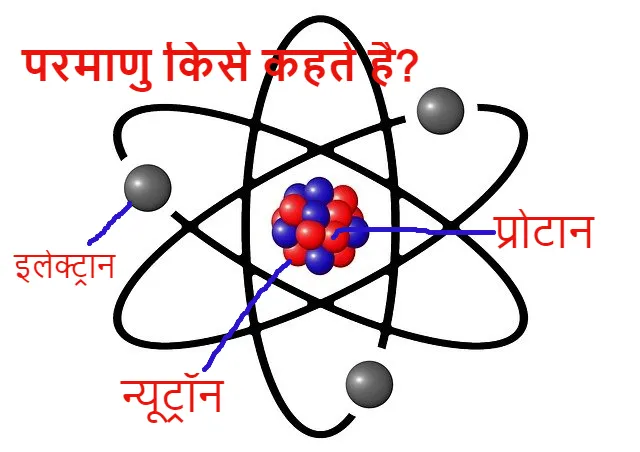
दोस्तों क्या आप जानना चाहते हैं कि संकरण किसे कहते है? यदि हां तो यह लेख सिर्फ आपके लिए ही है क्योंकि इस लेख में हम इसकी परिभाषा, प्रकार, विशेषताएं और उदाहरण के बारे में जानेंगे, तो चलिए बिना समय बर्बाद किया शुरू करते हैं।
संकरण किसे कहते है? (What is Hybridization in Hindi)
संकरण (Hybridization) –
किसी परमाणु की बाह्यतम कक्ष के भिन्न – भिन्न ऊर्जा के दो या दो से अधिक परमाणु कक्षक जब परस्पर जुड़कर समान ऊर्जा के दो या दो से अधिक नए कक्षक बनाते है तो इस प्रक्रिया को परमाणु कक्षको का संकरण कहते है और नई कक्षों को संकरित कक्षक कहते है, किसी परमाणु के n कक्षको के संकरण से n संकरण बनते है, संकरण कक्षक से अल्फा बंध बनते हो।
जैसे – कार्बन का मूल इलेक्ट्रानिक विन्यास निम्नलिखित है।
6C = 1s2, 2s2 2px¹ 2py¹ 2pz0 (तलस्थ अवस्था)
| ↑↑ |
| ↑ | ↑ |
या
| ↑↑ |
इसमें केवल दो संयोजी इलेक्ट्रान है, जबकि चार संयोजी इलेक्ट्रान होनी चाहिए क्योकि कार्बन की संयोजकता चार होती है यह माना जाता है कि 2s इलेक्ट्रानो में से एक इलेक्ट्रान उत्तेजित होकर pz कक्षक में चला जाता है अतः इलेक्ट्रानिक विन्यास अग्रांकित होता है –
6C = 1s2, 2s2 2px¹ 2py¹ 2pz1 (उत्तेजित अवस्था)
| ↑↑ |
| ↑ | ↑ | ↑ |
या
| ↑↑ |
ये चारो संयोजकताये समान नहीं है क्योकि s व p कक्षको की उर्जाये भिन्न – भिन्न होती है इस कारण ये चारो इलेक्ट्रान कक्षक मिश्रित होकर चार नये कक्षक बनाते है, जो सब समान होते है। ये चारो कक्षक समचतुष्फलक के चारो कोनों की ओर निर्देशित होते है और कार्बन परमाणु केंद्र पर स्थित होता है किन्ही दो कक्षको के बीच 109 Degree 28’ का कोण होता है।
संकरण की विशेषताए :–
संकरण की निम्नलिखित विशेषताए है।
- संकरण हमेशा परमाणु की बाह्यतम कक्ष के कक्षको का होता है संकरण का इलेक्ट्रानो से कोई समबन्ध नही होता है।
- संकरित कक्षको की निश्चित ज्यामितीय संरचना होती है।
- आधे भरे हुए कक्षक संकरण में भाग ले सकते है, परन्तु कभी – कभी अपूर्ण कक्षको के साथ पूर्ण भरे कक्षक भी भाग लेते है।
- जो परमाणु कक्षक संकरण से बनते है उनकी ऊर्जा समान होती है।
- जब कोई संकरित कक्षक अतिव्यापन द्वारा सहसंयोजक बंध बनाता है तो वह बंध हमेशा सिग्मा बंध होता है
- जितने परमाणु कक्षको को मिलाकर संकरण करते है उतने ही संकरित कक्षक बनते है।
- संकरित कक्षको में दिशात्मक गुण अधिक होता है अतः ये प्रबल बंध बनाते है।
- यह आवश्यक नहीं है कि बाह्यतम कक्ष के सभी अपूर्ण कक्षक संकरण में भाग लेते हों, बल्कि इनमे से कुछ कक्षक भी संकरण में भाग ले सकते है अतः ऐसे बचे हुए कक्षको को असंकरित कक्षक कहते है जो p या d कक्षक होते है तथा ये पार्श्व अतिव्यापन द्वारा हमेशा π – बंध बनाते है।
अभी तक तो हमने संकरण और संकरण की विशेषताओ के बारे में जाना है अब हम लोग संकरण के प्रकार के बारे में भी जान लेते है।
संकरण कितने प्रकार के होते है? (How many type Hybridization in hindi?)
संकरण के प्रकार – संकरण के कुछ मुख्य प्रारूप निम्नलिखित है।
sp – संकरण :–
जब एक s कक्षक तथा एक p कक्षक आपस में जुड़कर समान ऊर्जा के दो नए कक्षक बनाते है तो इस प्रक्रिया को sp – संकरण कहते है, और इस प्रकार के संकरण से बने समान ऊर्जा के कक्षक sp – संकर कक्षक कहलाते है। इस प्रकार का संकरण CO2, C2H2आदि में पाया जाता है। इन अणुओं की आकृति रेखीय होती है ये संकर कक्षक एक – दूसरे के साथ 180 डिग्री का कोण बनाते है।
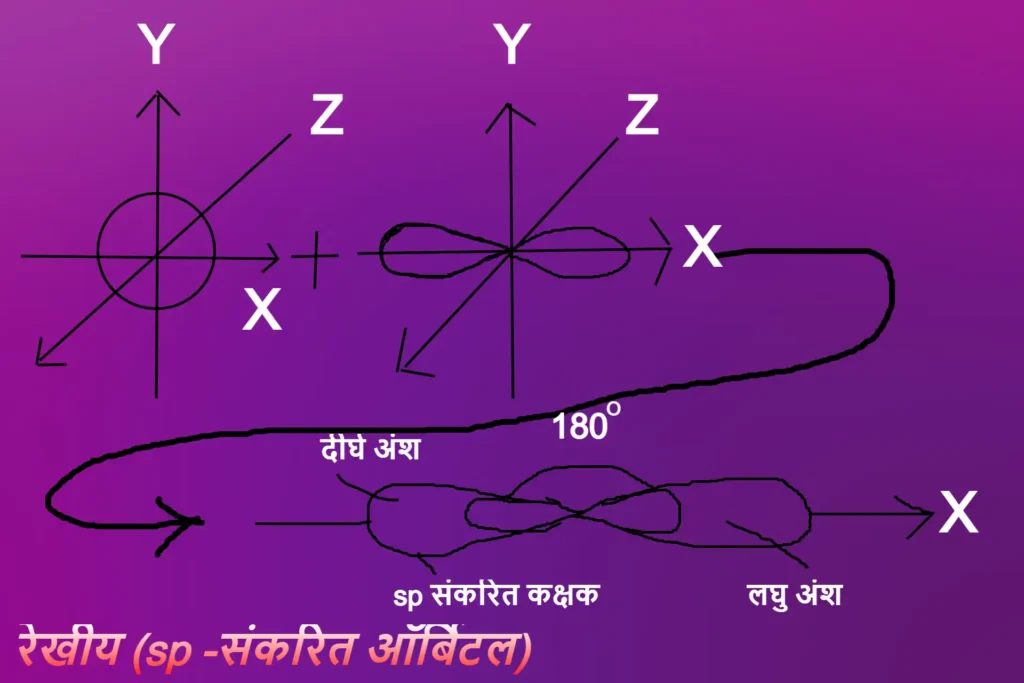
उदाहरण – ऐसीटिलिन (C2H2) के अणु में दोनों कार्बन परमाणु sp – संकरित है जिसके कारण C2H2 की संरचना रेखीय है। इस अणु में दोनों कार्बन परमाणुओं में sp – संकरित कक्षक (जो परस्पर बधी रहती है) तथा दो असंकरित p कक्षक होती है।
इनमे प्रत्येक कार्बन का एक – एक sp – संकरित कक्षक हाइड्रोजन के s- कक्षक से अपने अक्षों पर अतिव्यापन करके C – H के रूप में सिग्मा बंध का निर्माण करता है जबकि एक sp- संकरित कक्षक अपने अक्षों पर परस्पर अतिव्यापन द्वारा C – C के मध्य सिग्मा बंध का निर्माण करते है। दोनों परमाणुओं के शेष असंकरित p – कक्षक पार्श्व रूप में अतिव्यापन से पाई बंधो का निर्माण आगे लिखे गये प्रकार से करते है। इसमें H – C – C बंध 180 डिग्री होता है।
इसी प्रकार HgCl2, CO2 आदि अणुओं का निर्माण sp – संकरण द्वारा होता है
sp2 -संकरण :–
जब एक s कक्षक और दो p कक्षक आपस में परस्पर जुड़कर समान ऊर्जा के तीन नए कक्षक बनाते है तो इस प्रक्रिया को sp2 संकरण कहते है और इस प्रकार के संकरण से बने समान ऊर्जा के कक्षक sp2 संकर कक्षक कहलाते है। इस प्रकार का संकरण C2H4, C6H6 आदि में पाया जाता है। इस प्रकार के संकर कक्षको की आकृति त्रिकोणीय होती है।
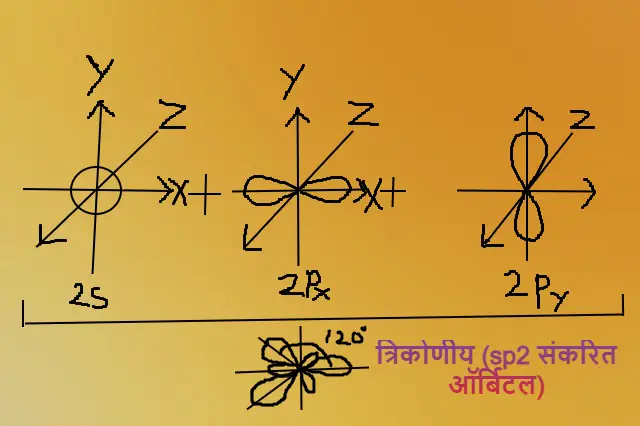
एथिलीन (C6H4) के अणु में दोनों कार्बन परमाणु sp2 संकरित है जिसके कारण C2H4की संरचना त्रिकोणीय होती है।इस अणु में दोनों कार्बन परमाणुओं में तीन sp2 संकरित तथा एक p असंकरित कक्षक दो – दो हाइड्रोजन परमाणुओं के s -कक्षको द्वारा उनके अक्षो पर अतिव्यापन से C – H बंध का सिग्मा बंध के रूप में निर्माण करते है।
प्रत्येक के एक – एक sp2 -संकरित कक्षक अपने अक्षो पर परस्पर अतिव्यापन से C – C बंध का सिग्मा बंध के रूप में निर्माण करते है। दोनों परमाणुओं के शेष एक – एक p -असंकरित कक्षक पार्श्व रूप में अतिव्यापन से पाई बंधो का निर्माण उपर्युक्त प्रकार से करते है इसमें H – C – C बंध लगभग 120 डिग्री का होता है।
इसके अतिरिक्त SO2, BCl3, SO3 आदि अणु भी sp2संकरण के द्वारा बनते है।
sp3 -संकरण :–
जब एक s कक्षक और तीन p कक्षक परस्पर आपस में जुडकर समान ऊर्जा के चार नए कक्षक बनाते है तो इस प्रक्रिया को sp3 -संकरण कहते है, और इस प्रकार के संकरण से बने समान ऊर्जा के कक्षक sp3 संकर कक्षक कहलाते है। इस प्रकार का संकरण CH4, CCl4 आदि अणुओं में पाया जाता है। इन अणुओं की आकृति चतुष्फलकीय होती है।
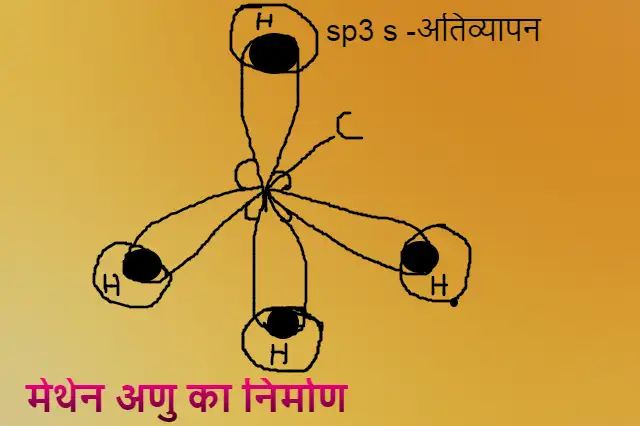
Example –
मेंथेन (CH4) के अणु में विद्यमान कार्बन परमाणु sp3 संकरित है जिसके कारण CH4अणु की संरचना चतुष्फलकीय होती है।
इस अणु में विद्यमान कार्बन परमाणुओं में चार sp2 संकरित कक्षक है जो परस्पर चतुष्फलक द्वारा जुड़े है। ये चार हाइड्रोजन परमाणुओं के चार s कक्षको द्वारा उनके अक्षो पर अतिव्यापन द्वारा चार C – H बंध का सिग्मा बंध के रूप में निर्माण करते है। इसमें H – C – H कोण लगभग 109 डिग्री 28’ का होता है।
इसके अतिरिक्त SO42– आयन PO43- आयन तथा SiCl4 आदि का निर्माण sp3 संकरण द्वारा होता है।
निष्कर्ष :-
दोस्तों आशा करता हूँ कि संकरण किसे कहते है? के बारे में दी गई जानकारी अच्छी लगी होगी दोस्तों यदि यह जानकारी अच्छी लगी है तो प्लीज इसे अपने दोस्तों के साथ ज्यादा से ज्यादा शेयर कीजिये।
NEET या दूसरे बोर्ड Exams के लिए कम्पलीट नोट्स बुक –
NEET Teachers के द्वारा एकदम सरल भाषा में लिखी गई नोट्स बुक 3 in 1, यानि कि एक ही किताब में जीव विज्ञान, रसायन विज्ञान और भौतिक विज्ञान की कम्पलीट कोर्स। यदि आपको इसकी जरूरत है तो नीचे दिए गये बुक इमेज पर क्लिक कीजिये और इसके बारे में और भी जानिए।
Thank you very much
इन्हें भी पढ़े :-
क्वांटम संख्या किसे कहते है? What is Quantum Number in hindi?
आफबाऊ का नियम क्या है? Aufbau Principle in Hindi?